Escolar Documentos
Profissional Documentos
Cultura Documentos
Transportadores de Influxo e Efluxo
Enviado por
Juan VelosoDireitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Transportadores de Influxo e Efluxo
Enviado por
Juan VelosoDireitos autorais:
Formatos disponíveis
1.1.1.1.
1 Transportadores de Influxo e Efluxo
Transportadores, expressos amplamente em todos os tecidos do corpo,
tem importante papel na absorção, distribuição, endereçamento de fármacos
tecido-específicos, influenciando assim na farmacocinética e farmacodinâmica
66
. Sendo assim, a sua expressão e atividade regula a habilidade de alguns
fármacos serem absorvidos a partir do intestino delgado, ou acessar orgãos,
impactando na eficácia desses em alcançar o seu alvo terapêutico e também
na sua toxicidade 65.
A maioria dos transportadores de influxo responsáveis pelo transporte
de xenobióticos pertence à superfamília SLC (Solute Carrier Transporter).
Nessa, primariamente foram caracterizadas 43 famílias de transportadores
diferentes, com um variado número de membros cada 67
, e hoje em dia, a lista
foi atualizada para 52 famílias diferentes, obtidas a partir de 395 genes
humanos68. OATPs (Organic Anion transporting polypeptides) são membros da
família SLC21/SLCO, OCTs (Organic cation transporter), da família SLC22 69, 70
e MATEs, da família SLC47 66.
Os OATPs mediam um transporte independente de sódio de uma ampla
gama de compostos orgânicos anfipáticos. Seu mecanismo de transporte
consiste na troca de um ânion, acoplando o influxo celular do substrato com o
efluxo de substâncias endógenas intracelulares, como bicarbonato, num
mecanismo eletroneutro. OCTs transportam cátions orgânicos de baixa massa
molecular e relativa hidrofilicidade 71. MATEs secretam cations e zwitterions
na urina, trabalhando como cátion/H+ antiporte em conjunto com OCT2,
localizado na membrana basolateral das células do túbulo proximal renal 66.
A maioria das proteínas que medeiam o efluxo de fármacos e seus
metabólitos para fora das células pertencem à superfamília ABC. A família de
transportadores ABC humanos contém 49 membros com 7 subfamílias
incluindo vários importantes transportadores de xenobióticos como a P-gp
(ABCB1), MRP 1-9 (ABCC10-12) e BRCP (ABCG2). Os transportadores ABC,
abundantes na membrana apical dos enterócitos, bombeiam ativamente
diversos substratos, incluindo aminoácidos, peptídeos, proteínas, lipídios,
sacarídeos, íons inorgânicos, metais e xenobióticos do interior das células. O
transporte dos substratos ocorre contra o gradiente de concentração, com o
gasto de ATP 72.
Especialistas em biotransformação, biotransporte e farmacocinética se
reuniram no “International Transporter Consortium” (ITC), com o objetivo de
discutir e identificar quais transportadores seriam determinantes bem
estabelecidos na farmacocinética, clinicamente importantes na absorção e
biodisponibilidade de fármacos, e consequentemente poderiam ser alvos de
interações medicamentosas. Em março de 2010, foi publicado o review “
Membrane transporters in drug development” 71
, ressaltando sete
transportadores que todos os membros concordaram que há evidências de
estarem envolvidos na absorção, biodisponibilidade e/ou interações
medicamentosas. São eles: P-gp (Glicoproteína P – MDR1, ABCB1), BCRP
(Breast Cancer Resistance Protein – ABCG2), OCT2 (SLC22A2), OAT1/OAT3
(Organic Anion Transporters, SLC22A6/SLC22A7) e OATP1B1 e OATP1B3
(SLCO1B1 E SLCO1B3).
Em 2013, uma atualização desses transportadores foi realizada pelo ITC
e publicada, tendo incluído nessa listagem MATE1 e MATE2/MATE2K como
envolvidos em interações fármaco-fármaco e implicados na eficácia e
toxicidade induzida por fármaco 66.
Dentre os transportadores considerados pelo ITC como clinicamente
importantes na biodisponibilidade de fármacos, dos quais os antidiabéticos em
estudo são substratos estão: P-gp, BCRP, OCT2, OATP1B1, OATP1B3,
MATE1 e MATE2-K66,71,73,74. Além disso, alguns estudos, apesar de
controversos, sugerem que variações genéticas em OCT1 podem ser
determinantes na variabilidade interindividual da biodisponibilidade da
metformina71,75. Stage e colaboradores (2016) apontaram a associação do uso
da codeína, um inibidor de OCT1, a um risco aumentado de descontinuação
precoce da metformina76.
Em humanos, OATP1B1 e OATP1B3 estão ampla e exclusivamente
expressos na membrana basolateral dos hepatócitos 73.
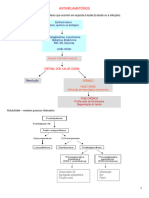
Figura 8: : Transportadores selecionados para a investigação das interações e suas localizações.
Fonte: Figura construída basseada nas informações em 66,71,78.
OCT1 é expresso principalmente no fígado, na membrana basolateral
dos hepatócitos, mas pode estar fracamente expresso em outros locais, como
intestino delgado, cólon, rins , pulmão, cérebro, coração, músculo esquelético,
leucócitos periféricos, glandula adrenal e mamária, células imunes e tecido
adiposo70.
OCT2 é predominantemente expresso na membrana basolateral das
células do túbulo proximal renais, e fracamente expresso no cérebro, pulmão,
intestino delgado, timo, placenta e ouvido interno 70.
MATE1 é altamente expresso no fígado, rins, glândula adrenal e
músculo esquelético, estando localizado na membrana apical das células do
túbulo proximal renal e dos hepatócitos. MATE2/MATE2-K são expressos
principalmente nos rins, onde estão restritos à membrana apical das células do
túbulo proximal renal 70.
P-gp está expressa na membrana luminal (também chamada apical) dos
enterócitos do intestino delgado, na barreira hemato-encefálica, na membrana
apical dos hepatócitos e no epítélio do túbulo proximal renal 71.
BCRP é amplamente expressa na membrana luminal dos enterócitos 74
,
mas também ocorre nos hepatócitos, rim, endotélio cerebral, tecido mamário,
testículos e placenta 71.
Apesar de PMAT (Plasma membrane monoamine transporter) ser um
dos transportadores, localizado na membrana apical dos enterócitos,
responsáveis pelo transporte da metformina a partir do trato gastrointestinal 75,77
, ou seja, teoricamente com importante influência na biodisponibilidade de
medicamentos da Classe 3 BDDCS, ele não foi identificado pelo ITC como
biotransportador com importantes implicações clínicas 66.
A Error: Reference source not found ilustra as localizações dos
transportadores relevantes aos antidiabéticos, nos hepatócitos, enterócitos e
células renais (Metabolismo Fase 0 e III). Os transportadores e suas ações,
antidiabéticos deles substratos e o resultado esperado da sua inibição ou
indução estão descritos no Quadro 1.
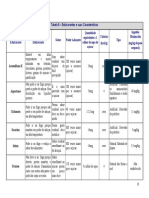
Quadro 1: Transportadores potencialmente influentes na farmacocinética dos antidiabéticos e
efeitos da sua inibição/indução
Gene/ Transport Medicamento Efeito previsto da
Localização Ação Ref.
Família a dor afetado inibição (indução)
Glibenclamida Metabolismo 65,73
reduzido
SLCO1B
OATP1B1 Repaglinida, (aumentado),
1/ 73
e Influxo Nateglinida exposição ao
SLCO1B
OATP1B3 fármaco original
3
aumentada 69
Membrana Pioglitazona (reduzida)
basolateral
dos Exposição
hepatócitos aumentada
(diminuída) ao
65,70,71
SLC22A fármaco original, a
OCT1 Influxo Metformina
1 inibição diminui seus ,76,78
níveis intracelulares,
prejudicando sua
farmacodinâmica
Membrana ABCB1 e P-gp e Efluxo Glibenclamida Metabolismo 65,74
apical ABCG2 BCRP aumentado
(canalicular) (reduzido),
dos exposição ao
hepatócitos fármaco original
reduzida
(aumentada)
Exposição hepática
ao fármaco
aumentada 65,66,71
SLC47A
MATE1 Efluxo Metformina (diminuída),
1 ,78,79
diminuição
(aumento) da
excreção biliar
Metabolismo
reduzido
Membrana (aumentado), 65,66,69
ABCB1 e P-gp e
apical dos Efluxo Glibenclamida exposição ao
ABCG2 BCRP ,71,74
enterócitos fármaco original
aumentada
(diminuída)
Membrana Exposição
65,71,75
basolateral SLC22A aumentada
OCT1 Influxo Metformina
dos 1 (diminuída) ao ,80
enterócitos fármaco
A inibição causa
Membrana diminuição no
basolateral clearance renal e
66,71
,
SLC22A 78
do túbulo OCT2 Influxo Metformina aumento na
2
proximal exposição ao
renal fármaco em estudos
clínicos
A inibição de MATE1
Membrana e MATE2-K causa
SLC47A
apical do MATE1, diminuição no 65,71,75
1e
túbulo MATE2 E Efluxo Metformina clearance renal e
proximal
SLC47A
MATE2-K aumento na ,78
2
renal exposição em
estudos clínicos
Membrana
basolateral
66,71,74
do túbulo ABCB1 P-gp Efluxo Glibenclamida ...
proximal
renal
Você também pode gostar
- Guia de Prescrição de Probióticos Ana Paula PujolDocumento44 páginasGuia de Prescrição de Probióticos Ana Paula PujolEmily Barreto50% (2)
- Exercícios Técnica PICODocumento2 páginasExercícios Técnica PICOJoão Vitor100% (1)
- Material de Estudo QF1Documento23 páginasMaterial de Estudo QF1ThayanaTabarkiewiczAinda não há avaliações
- Programa Diabetes Controlada DR RochaDocumento2 páginasPrograma Diabetes Controlada DR Rochawileyqjdhktputg0% (2)
- Aula 2Documento5 páginasAula 2Marcos CarvalhoAinda não há avaliações
- AinesatualDocumento25 páginasAinesatualisabelly martinsAinda não há avaliações
- Fisiopatologia Diabetes Mellitus Tipo 2Documento34 páginasFisiopatologia Diabetes Mellitus Tipo 2Regina Celia100% (1)
- SNA - Parte I - Profa Nívea NevesDocumento84 páginasSNA - Parte I - Profa Nívea NevestitigarproAinda não há avaliações
- FARMACODINÂMICADocumento11 páginasFARMACODINÂMICAPedro Henrique Cavalcante de SouzaAinda não há avaliações
- Aula Doenças Pancreáticas Gabanutri PDFDocumento70 páginasAula Doenças Pancreáticas Gabanutri PDFDaniele Andreia AlvaresAinda não há avaliações
- Aula - Screening de InibidoresDocumento10 páginasAula - Screening de Inibidoresjheniiffer19Ainda não há avaliações
- NEFRO - AULA 3 - Fisio RenalDocumento11 páginasNEFRO - AULA 3 - Fisio Renaljaisa.santana01Ainda não há avaliações
- Mecanismo de Ação Dos FarmacosDocumento28 páginasMecanismo de Ação Dos FarmacosNatã DiasAinda não há avaliações
- ABV Aula 4 - 3 - TetraciclinasDocumento1 páginaABV Aula 4 - 3 - TetraciclinasLidianeHelenaAinda não há avaliações
- Albatin Literatura (trp-2)Documento7 páginasAlbatin Literatura (trp-2)WALACEAinda não há avaliações
- Aula 3 - Eicosanóides e Aines - DPDocumento48 páginasAula 3 - Eicosanóides e Aines - DPTalita EstefaniAinda não há avaliações
- Receptores AdrenérgicosDocumento8 páginasReceptores AdrenérgicosMarcelo100% (1)
- AinesDocumento41 páginasAinesZilmar Oliveira100% (1)
- Atividade Bimestral 1 de Bff1 4ºpDocumento5 páginasAtividade Bimestral 1 de Bff1 4ºpdeboraunirAinda não há avaliações
- Dislipidemias E Distúrbios Do Metabolismo Das Lipoproteínas: Edicina ElevânciaDocumento50 páginasDislipidemias E Distúrbios Do Metabolismo Das Lipoproteínas: Edicina ElevânciaRita MendesAinda não há avaliações
- Acox-2+dipirona+dexa+paracetamol-Nimesulida-Cetoprofeno - AL + Dexa + Clonidina-2020Documento54 páginasAcox-2+dipirona+dexa+paracetamol-Nimesulida-Cetoprofeno - AL + Dexa + Clonidina-2020Bruno Henrique DarozAinda não há avaliações
- 347-Texto Do Artigo-318-1-10-20130725Documento2 páginas347-Texto Do Artigo-318-1-10-20130725Lorena RosaAinda não há avaliações
- Quadro ResumoDocumento2 páginasQuadro ResumoVitor PontesAinda não há avaliações
- Paracetamol PDFDocumento4 páginasParacetamol PDFElizandra AlvesAinda não há avaliações
- Revisão SinalizaçãoDocumento16 páginasRevisão SinalizaçãoJucicléia NatháliaAinda não há avaliações
- Aula 3 FarmacodinamicaDocumento45 páginasAula 3 FarmacodinamicaViviane LimaAinda não há avaliações
- Resumão Da POHA - Sinalização MolecularDocumento202 páginasResumão Da POHA - Sinalização Moleculardavi2002ramalhoAinda não há avaliações
- Aies SC 2019.Documento9 páginasAies SC 2019.Ana Paula Silva CruzAinda não há avaliações
- Memorex de FarmacologiaDocumento9 páginasMemorex de FarmacologiaAriniceCostaAinda não há avaliações
- Fasciculo Epilepsia - Inducao EnzimaticaDocumento12 páginasFasciculo Epilepsia - Inducao Enzimaticasammy_emerichAinda não há avaliações
- Resumo Farmaco Parte 1Documento11 páginasResumo Farmaco Parte 1Adilson GomesAinda não há avaliações
- Farmaco - Anti-InflamatóriosDocumento13 páginasFarmaco - Anti-InflamatóriosMarcusVeniciusAinda não há avaliações
- Resumo - Proteínas Plasmáticas - Bioquímica ClínicaDocumento22 páginasResumo - Proteínas Plasmáticas - Bioquímica ClínicaThatianaGouveia100% (1)
- Fisiopatologia Diabetes Mellitus Tipo 2Documento34 páginasFisiopatologia Diabetes Mellitus Tipo 2paulo100% (1)
- 3 - Modelo Carteziando Do Mecanismo de Acao AuxinasDocumento36 páginas3 - Modelo Carteziando Do Mecanismo de Acao AuxinasZuleide Silva de CarvalhoAinda não há avaliações
- RosuvastatinaDocumento2 páginasRosuvastatinapowerq3Ainda não há avaliações
- Dislipidemias LipidogramaDocumento14 páginasDislipidemias Lipidogramamaria eduardaAinda não há avaliações
- En Zimo GramaDocumento148 páginasEn Zimo GramaAlberto Frazão Treinador & NutricionistaAinda não há avaliações
- Farm Acolo Gia SoiDocumento9 páginasFarm Acolo Gia SoiLucas AssisAinda não há avaliações
- Influxo EfluxoDocumento3 páginasInfluxo EfluxoJuan VelosoAinda não há avaliações
- Tecido Adiposo Clinica IntegradaDocumento28 páginasTecido Adiposo Clinica IntegradaJuan AnzeAinda não há avaliações
- Níveis Plasmáticos de TaurinaDocumento5 páginasNíveis Plasmáticos de TaurinaSeção de Beneficiamento Fazenda da AeronáuticaAinda não há avaliações
- Sais Biliares PDFDocumento3 páginasSais Biliares PDFSilviane SilvérioAinda não há avaliações
- ED - Anti-InflamatóriosDocumento2 páginasED - Anti-InflamatóriosMatheus PontesAinda não há avaliações
- Diabetes Mellitus Tipo 2 e Sind MetabólicaDocumento43 páginasDiabetes Mellitus Tipo 2 e Sind MetabólicaYzabel Basílio100% (1)
- Reprodução RESUMO ARTIGoDocumento5 páginasReprodução RESUMO ARTIGoprimodieliAinda não há avaliações
- SinalizaçãoDocumento4 páginasSinalizaçãoMariana PaesAinda não há avaliações
- Aula Doenças Pancreáticas Gabanutri PDFDocumento71 páginasAula Doenças Pancreáticas Gabanutri PDFDaniele Andreia AlvaresAinda não há avaliações
- Bartold2006 en PTDocumento21 páginasBartold2006 en PTJúlia OliveiraAinda não há avaliações
- BerberinaDocumento1 páginaBerberinaAmanda KrügerAinda não há avaliações
- Efeitos Pleiotrópicos Das EstatinasDocumento52 páginasEfeitos Pleiotrópicos Das EstatinasIsabela Stoffle da Silva100% (1)
- VasopressinaDocumento6 páginasVasopressinaLuis FernandoAinda não há avaliações
- The Impact of Diet Upon Mitochondrial PhysiologyDocumento26 páginasThe Impact of Diet Upon Mitochondrial PhysiologyGuilherme StrunckAinda não há avaliações
- PretClinica CorticoideDocumento28 páginasPretClinica CorticoideChaquir Ossifo AtumaneAinda não há avaliações
- Farmacologia - AntileishmaniaDocumento2 páginasFarmacologia - AntileishmaniaKamila BarretoAinda não há avaliações
- FarmacologiaDocumento11 páginasFarmacologiacamila.gnoronhaAinda não há avaliações
- ALA - Efeitoadverso Altas Doses para Mitocondria Do FigadoDocumento3 páginasALA - Efeitoadverso Altas Doses para Mitocondria Do FigadokarllozaraujoAinda não há avaliações
- Atividade 3 - Bio - Bioquímica Clínica - 51-2023Documento2 páginasAtividade 3 - Bio - Bioquímica Clínica - 51-2023Cavalini Assessoria AcadêmicaAinda não há avaliações
- Estudo Transversal AteroscleroseDocumento10 páginasEstudo Transversal AteroscleroseHigor RairAinda não há avaliações
- Captura de Tela 2024-02-29 À(s) 16.56.35Documento3 páginasCaptura de Tela 2024-02-29 À(s) 16.56.35Gabriele EngediAinda não há avaliações
- Capitulo 4 - 57-66p - Hepatico - Pancreas - RumenDocumento10 páginasCapitulo 4 - 57-66p - Hepatico - Pancreas - Rumenyonemonsores.alunoAinda não há avaliações
- Prolactina e Diabetes Melito do tipo 2: o efeito protetor de um hormônio sobre o metabolismo glicídicoNo EverandProlactina e Diabetes Melito do tipo 2: o efeito protetor de um hormônio sobre o metabolismo glicídicoAinda não há avaliações
- GUIA 0 A 2 AnosDocumento62 páginasGUIA 0 A 2 AnosJuan VelosoAinda não há avaliações
- Obesidade Infantil 1890Documento17 páginasObesidade Infantil 1890Juan VelosoAinda não há avaliações
- Livro Pintura PDFDocumento132 páginasLivro Pintura PDFJuan VelosoAinda não há avaliações
- Cópia de Fomulas - Infantis - e - Codex - AlimentariusDocumento31 páginasCópia de Fomulas - Infantis - e - Codex - AlimentariusHérika MartinsAinda não há avaliações
- Aula 11 Nutrição InfantilDocumento83 páginasAula 11 Nutrição InfantilJuan VelosoAinda não há avaliações
- Cartilha Orientacao Nutricional 12-03-13Documento33 páginasCartilha Orientacao Nutricional 12-03-13Claudia Senise de JesusAinda não há avaliações
- InteraçãoDocumento8 páginasInteraçãoJuan VelosoAinda não há avaliações
- Cite As 3 Casas de Submúltiplos Da Unidade de Medida GramaDocumento1 páginaCite As 3 Casas de Submúltiplos Da Unidade de Medida GramaJuan VelosoAinda não há avaliações
- Azdoc - Tips Apostilas em PDF Do Senai 03 Ts Pintura PDFDocumento10 páginasAzdoc - Tips Apostilas em PDF Do Senai 03 Ts Pintura PDFJuan VelosoAinda não há avaliações
- Alimentacao Saudavel CriançasDocumento8 páginasAlimentacao Saudavel CriançasJuan Veloso100% (1)
- Aula 10 Alimentação ComplementarDocumento37 páginasAula 10 Alimentação ComplementarJaqueline MoreiraAinda não há avaliações
- Alimentos Recomendados para Bebês de 0 A 6 Meses de IdadeDocumento4 páginasAlimentos Recomendados para Bebês de 0 A 6 Meses de IdadeFlavia Rodrigues dos Santos de PaulaAinda não há avaliações
- Manual Pintura. PDFDocumento26 páginasManual Pintura. PDFJuan VelosoAinda não há avaliações
- Apostila de Atividades Alimentação Saudável 6° Ao 9º Ano PDFDocumento28 páginasApostila de Atividades Alimentação Saudável 6° Ao 9º Ano PDFAryanne Alves83% (6)
- Apostila de Atividades Alimentação Saudável 1° Ao 5º Ano PDFDocumento28 páginasApostila de Atividades Alimentação Saudável 1° Ao 5º Ano PDFJefferson BárbaraAinda não há avaliações
- Alimentacao SaudavelDocumento35 páginasAlimentacao Saudavelelisalontro8937Ainda não há avaliações
- Alimentação No Primeiro Ano de Vida (Hospital e Maternidade de Embu)Documento4 páginasAlimentação No Primeiro Ano de Vida (Hospital e Maternidade de Embu)Juan VelosoAinda não há avaliações
- Alimentação Complementa OrientçõesrDocumento6 páginasAlimentação Complementa OrientçõesrJuan VelosoAinda não há avaliações
- PRESENTE 10 - AdeusRegimeEbook-20150924-222056Documento47 páginasPRESENTE 10 - AdeusRegimeEbook-20150924-222056GIBI Brasil-germanoAinda não há avaliações
- Alimentação Infantil - Bases FisiológicasDocumento102 páginasAlimentação Infantil - Bases FisiológicasJullian Thales Santos100% (1)
- Cartilha Alimentação InfantilDocumento86 páginasCartilha Alimentação InfantilEncarteReceitas100% (4)
- A Introdução Da Alimentação Complementar e Sua Relação Com A Obesidade InfantilDocumento12 páginasA Introdução Da Alimentação Complementar e Sua Relação Com A Obesidade InfantilJuan VelosoAinda não há avaliações
- A Química Dos AlimentosDocumento54 páginasA Química Dos Alimentosturma11ufmt100% (3)
- Leites VegetaisDocumento4 páginasLeites VegetaisMorgana GiattiAinda não há avaliações
- 31 2015 NutriçãoDocumento2 páginas31 2015 NutriçãoJuan VelosoAinda não há avaliações
- Acentuação - OrtografiaDocumento4 páginasAcentuação - OrtografiaJuan VelosoAinda não há avaliações
- Tabela de EdulcorantesDocumento3 páginasTabela de EdulcorantesDanyelle EmidioAinda não há avaliações
- Unid+3 +seção+1 +Sistema+HormonalDocumento26 páginasUnid+3 +seção+1 +Sistema+HormonalLudimyla AlmeidaAinda não há avaliações
- UntitledDocumento246 páginasUntitledJosé Carlos LippiAinda não há avaliações
- GuiamedicoDocumento19 páginasGuiamedicoCan EbeAinda não há avaliações
- Go PerguntasDocumento4 páginasGo PerguntasviniciuscabAinda não há avaliações
- Estudo Dirigido - Atuação Da Fisioterapia No Ambiente HospitalarDocumento2 páginasEstudo Dirigido - Atuação Da Fisioterapia No Ambiente HospitalarJuliana AssisAinda não há avaliações
- Tabela de DTASDocumento9 páginasTabela de DTASRaquel OliveiraAinda não há avaliações
- Med - Club DistúrbiosÁcidosBase ResumoDocumento15 páginasMed - Club DistúrbiosÁcidosBase Resumothayafer6Ainda não há avaliações
- Medidas de Associação - ODDS RatioDocumento16 páginasMedidas de Associação - ODDS RatioFabbio BaldoinoAinda não há avaliações
- PIIS2213858720303818Documento15 páginasPIIS2213858720303818JulianeAinda não há avaliações
- 01 Book Guia Medico Andradina 2020Documento52 páginas01 Book Guia Medico Andradina 2020Alisson Gomes DiasAinda não há avaliações
- AVC - Apresentação Internato PS (Pronto)Documento38 páginasAVC - Apresentação Internato PS (Pronto)Ana Luyza OliveiraAinda não há avaliações
- Microbiologia Clinica ApostilaDocumento89 páginasMicrobiologia Clinica ApostilaTania OliveiraAinda não há avaliações
- Migração Dos MelanócitosDocumento2 páginasMigração Dos MelanócitosMariana NetoAinda não há avaliações
- A Ceti Lci Stein A Granula Do EmsDocumento7 páginasA Ceti Lci Stein A Granula Do EmsKayo LorranAinda não há avaliações
- Aula Dia 16112020 PDFDocumento67 páginasAula Dia 16112020 PDFAryane FernandesAinda não há avaliações
- Transporte de Gases No SangueDocumento2 páginasTransporte de Gases No SangueMilene BabelesAinda não há avaliações
- Aula 1 EpidemiologiaDocumento81 páginasAula 1 EpidemiologiaDjoncy ChirrindzeAinda não há avaliações
- Od - Ped - 1CTDocumento7 páginasOd - Ped - 1CTMaria de LourdesAinda não há avaliações
- MelasmaDocumento61 páginasMelasmavinimarciaAinda não há avaliações
- Endocrinologia 2024Documento27 páginasEndocrinologia 2024amandamaronez53Ainda não há avaliações
- Osteoporose e Rizotomia Ou Microneurólise de Nervos GenicularesDocumento7 páginasOsteoporose e Rizotomia Ou Microneurólise de Nervos GenicularesCristi PrudenteAinda não há avaliações
- Epidemiologia 2017-1Documento102 páginasEpidemiologia 2017-1Eliabe AlmeidaAinda não há avaliações
- Avaliação Da Atividade Antitumoral Do Ipê-Roxo - Uma RevisãoDocumento12 páginasAvaliação Da Atividade Antitumoral Do Ipê-Roxo - Uma Revisãoedmilsonrochalira2Ainda não há avaliações
- Avaliacao de Prescricoes de Medicamentos A Luz Dos Criterios de Beers Fick No Centro de Atencao Especializada Do Idoso de Belem paraDocumento15 páginasAvaliacao de Prescricoes de Medicamentos A Luz Dos Criterios de Beers Fick No Centro de Atencao Especializada Do Idoso de Belem paraKeytiane JVAinda não há avaliações
- Menu Laser TransdérmicoDocumento4 páginasMenu Laser TransdérmicoAlexandre Campos Moraes AmatoAinda não há avaliações
- Exercício Resolvido - EpidemiologiaDocumento4 páginasExercício Resolvido - EpidemiologiaAnyrbas ReyemAinda não há avaliações