Escolar Documentos
Profissional Documentos
Cultura Documentos
Cefazolina Sódica
Enviado por
celmorcelliTítulo original
Direitos autorais
Formatos disponíveis
Compartilhar este documento
Compartilhar ou incorporar documento
Você considera este documento útil?
Este conteúdo é inapropriado?
Denunciar este documentoDireitos autorais:
Formatos disponíveis
Cefazolina Sódica
Enviado por
celmorcelliDireitos autorais:
Formatos disponíveis
Logo Empresa
FICHA DE REFERÊNCIA
INSUMO FARMACÊUTICO
Nome: Nº DCB Cód. DCB
Cefazolina sódica 01846 01442.02-3
Sinonímia: Nº CAS
Cefazolina de sódio 27164-46-1
Fórmula molecular: Peso molecular: Formas farmacêuticas
C14H13N8NaO4S3 476,49 usuais:
Forma química: Pós para soluções
Sal injetáveis
Fator de equivalência: Fator de correção:
1,05 Consultar o certificado de análise
da matéria-prima para verificar a
necessidade de aplicar o fator de
correção.
Usos:
Antibiótico bactericida de amplo espectro
Grau de pureza / aplicação:
Grau farmacêutico
Especificação Geral
Teor ou Potência: Mínimo de 89,1% e máximo de 110,1%, calculado em relação à substância anidra
Testes Básicos de Identificação
Características organolépticas: Pó branco ou quase branco, muito higroscópico
Solubilidade: Muito solúvel em água, ligeiramente solúvel em etanol e praticamente insolúvel em éter
etílico
Ponto de fusão: Não aplicável
Poder rotatório específico: Entre -10º e -24º
Densidade: Não aplicável
Identificação
Espectrofotometria de absorção no infravermelho, apresenta máximo de absorção somente nos mesmos
comprimentos de onda e com as mesmas intensidades relativas daqueles observados no espectro da
substância padrão
HPLC, o tempo de retenção do pico principal obtido com a solução da amostra corresponde àquele do
pico principal da solução padrão
Reação de íons sódio positiva
Ensaios de Pureza
pH: Entre 4,0 e 6,0 (Solução aquosa a 10%(p/V))
Água: No máximo 6,0%
Outros ensaios
Endotoxinas bacterianas: No máximo 0,25 EU/mg
Embalagem e Armazenamento
Armazenar em recipientes bem-fechados, entre 2º e 8º C
Amostragem
Verificar procedimento geral e/ou específico de amostragem.
Precauções
Observar descrito na FISPQ.
Referências
1. Farmacopéia Brasileira, 2003. p.222, 4a.ed
Elaborado por: Aprovado por:
CÓPIA CONTROLADA Data: Revisão nº: Nº de página:
de
Você também pode gostar
- QuímicaDocumento100 páginasQuímicamaria eduarda maiaAinda não há avaliações
- Procedimentos para Boa FermentacaoDocumento45 páginasProcedimentos para Boa FermentacaoAparecido RodriguesAinda não há avaliações
- M Pop OdontoDocumento23 páginasM Pop OdontoNewton AndradeAinda não há avaliações
- Despigmentantes (Modo de Compatibilidade) PDFDocumento10 páginasDespigmentantes (Modo de Compatibilidade) PDFTatiane Fernandes100% (1)
- Salicilato de Metila - Relatório IDocumento6 páginasSalicilato de Metila - Relatório IRenata GomesAinda não há avaliações
- Relatório Prática - Química Analítica Qualitativa CorrigidoDocumento4 páginasRelatório Prática - Química Analítica Qualitativa CorrigidoSecundária Freitas100% (1)
- Seminário Impermeabilização FlexívelDocumento25 páginasSeminário Impermeabilização FlexívelKaren Andrade100% (1)
- Cefoxitina SódicaDocumento1 páginaCefoxitina SódicacelmorcelliAinda não há avaliações
- Cloridrato de DifenoxilatoDocumento1 páginaCloridrato de DifenoxilatocelmorcelliAinda não há avaliações
- CimetidinaDocumento2 páginasCimetidinacelmorcelliAinda não há avaliações
- Sulfato de IndinavirDocumento1 páginaSulfato de IndinavircelmorcelliAinda não há avaliações
- ProbenecidaDocumento1 páginaProbenecidacelmorcelliAinda não há avaliações
- LamivudinaDocumento1 páginaLamivudinacelmorcelliAinda não há avaliações
- Ácido SórbicoDocumento1 páginaÁcido SórbicocelmorcelliAinda não há avaliações
- DidanosinaDocumento1 páginaDidanosinacelmorcelliAinda não há avaliações
- Ampicilina SódicaDocumento1 páginaAmpicilina SódicacelmorcelliAinda não há avaliações
- Valproato de SódioDocumento1 páginaValproato de SódiocelmorcelliAinda não há avaliações
- Estearato de EritromicinaDocumento1 páginaEstearato de EritromicinacelmorcelliAinda não há avaliações
- Cloridrato de FluoxetinaDocumento2 páginasCloridrato de FluoxetinacelmorcelliAinda não há avaliações
- Cloridrato de AmodiaquinaDocumento1 páginaCloridrato de AmodiaquinacelmorcelliAinda não há avaliações
- DigoxinaDocumento2 páginasDigoxinacelmorcelliAinda não há avaliações
- Fenitoína SódicaDocumento1 páginaFenitoína SódicacelmorcelliAinda não há avaliações
- CaptoprilDocumento1 páginaCaptoprilcelmorcelliAinda não há avaliações
- LidocaínaDocumento1 páginaLidocaínacelmorcelliAinda não há avaliações
- AciclovirDocumento1 páginaAciclovircelmorcelliAinda não há avaliações
- Cloridrato de RanitidinaDocumento1 páginaCloridrato de RanitidinacelmorcelliAinda não há avaliações
- Difosfato de PrimaquinaDocumento1 páginaDifosfato de PrimaquinacelmorcelliAinda não há avaliações
- BendroflumetiazidaDocumento1 páginaBendroflumetiazidacelmorcelliAinda não há avaliações
- Cloridrato de CodeínaDocumento1 páginaCloridrato de CodeínacelmorcelliAinda não há avaliações
- Cloridrato de EmetinaDocumento1 páginaCloridrato de EmetinacelmorcelliAinda não há avaliações
- PropiltiouracilDocumento1 páginaPropiltiouracilcelmorcelliAinda não há avaliações
- Cloridrato de SertralinaDocumento1 páginaCloridrato de SertralinacelmorcelliAinda não há avaliações
- Pravastatina SódicaDocumento1 páginaPravastatina SódicacelmorcelliAinda não há avaliações
- Nitrato de PilocarpinaDocumento1 páginaNitrato de PilocarpinacelmorcelliAinda não há avaliações
- Tartarato de MetoprololDocumento1 páginaTartarato de MetoprololcelmorcelliAinda não há avaliações
- CetoconazolDocumento1 páginaCetoconazolcelmorcelliAinda não há avaliações
- Nitrato de NafazolinaDocumento1 páginaNitrato de NafazolinacelmorcelliAinda não há avaliações
- FlunitrazepamDocumento1 páginaFlunitrazepamcelmorcelliAinda não há avaliações
- IsoniazidaDocumento1 páginaIsoniazidacelmorcelliAinda não há avaliações
- AlbendazolDocumento2 páginasAlbendazolcelmorcelliAinda não há avaliações
- NorfloxacinoDocumento1 páginaNorfloxacinocelmorcelliAinda não há avaliações
- CiclofosfamidaDocumento1 páginaCiclofosfamidacelmorcelliAinda não há avaliações
- MetilparabenoDocumento1 páginaMetilparabenocelmorcelliAinda não há avaliações
- Difosfato de DietilestilbestrolDocumento1 páginaDifosfato de DietilestilbestrolcelmorcelliAinda não há avaliações
- OfloxacinoDocumento1 páginaOfloxacinocelmorcelliAinda não há avaliações
- GenfibrozilaDocumento1 páginaGenfibrozilacelmorcelliAinda não há avaliações
- Monocloridrato de FlurazepamDocumento1 páginaMonocloridrato de FlurazepamcelmorcelliAinda não há avaliações
- Permanganato de Potássio GFDocumento1 páginaPermanganato de Potássio GFcelmorcelliAinda não há avaliações
- CiprofloxacinoDocumento1 páginaCiprofloxacinocelmorcelliAinda não há avaliações
- LevodopaDocumento1 páginaLevodopacelmorcelliAinda não há avaliações
- Calcitonina Sintética de SalmãoDocumento1 páginaCalcitonina Sintética de SalmãocelmorcelliAinda não há avaliações
- BromazepamDocumento1 páginaBromazepamcelmorcelliAinda não há avaliações
- Fenobarbital SódicoDocumento1 páginaFenobarbital SódicocelmorcelliAinda não há avaliações
- EsqualanoDocumento1 páginaEsqualanocelmorcelliAinda não há avaliações
- Sulfato de SalbutamolDocumento1 páginaSulfato de SalbutamolcelmorcelliAinda não há avaliações
- ClordiazepóxidoDocumento1 páginaClordiazepóxidocelmorcelliAinda não há avaliações
- Cefalotina SódicaDocumento1 páginaCefalotina SódicacelmorcelliAinda não há avaliações
- TenoxicamDocumento1 páginaTenoxicamcelmorcelliAinda não há avaliações
- FluconazolDocumento2 páginasFluconazolcelmorcelliAinda não há avaliações
- BacitracinaDocumento1 páginaBacitracinacelmorcelliAinda não há avaliações
- Cloridrato de HidralazinaDocumento1 páginaCloridrato de HidralazinacelmorcelliAinda não há avaliações
- BisacodilDocumento1 páginaBisacodilcelmorcelliAinda não há avaliações
- Caprilato de SódioDocumento1 páginaCaprilato de SódiocelmorcelliAinda não há avaliações
- ColchicinaDocumento2 páginasColchicinacelmorcelliAinda não há avaliações
- Sulfato de HidroxocobalaminaDocumento1 páginaSulfato de HidroxocobalaminacelmorcelliAinda não há avaliações
- FurosemidaDocumento2 páginasFurosemidacelmorcelliAinda não há avaliações
- Correlação In Vitro – In Vivo no Desenvolvimento de MedicamentosNo EverandCorrelação In Vitro – In Vivo no Desenvolvimento de MedicamentosAinda não há avaliações
- Imidazolidinil UréiaDocumento1 páginaImidazolidinil UréiacelmorcelliAinda não há avaliações
- Lit OLEO OLIVA VIRGEM AMIDocumento1 páginaLit OLEO OLIVA VIRGEM AMIcelmorcelliAinda não há avaliações
- Óleo Essencial de Breu BrancoDocumento1 páginaÓleo Essencial de Breu BrancocelmorcelliAinda não há avaliações
- Esferas de JojobaDocumento1 páginaEsferas de JojobacelmorcelliAinda não há avaliações
- Manteiga de UcuubaDocumento1 páginaManteiga de UcuubacelmorcelliAinda não há avaliações
- Fisio LESA LSADocumento2 páginasFisio LESA LSAcelmorcelliAinda não há avaliações
- Acido LacticoDocumento1 páginaAcido LacticocelmorcelliAinda não há avaliações
- Barbatimao FenixDocumento1 páginaBarbatimao FenixcelmorcelliAinda não há avaliações
- Boletim BetulaDocumento1 páginaBoletim BetulacelmorcelliAinda não há avaliações
- Lanolina-Anidra EmfalDocumento1 páginaLanolina-Anidra EmfalcelmorcelliAinda não há avaliações
- Lit GOMA XANTANADocumento1 páginaLit GOMA XANTANAcelmorcelliAinda não há avaliações
- Oleo de GirassolDocumento1 páginaOleo de GirassolcelmorcelliAinda não há avaliações
- MequinolDocumento2 páginasMequinolcelmorcelliAinda não há avaliações
- Baunilha HG 10785 LitDocumento1 páginaBaunilha HG 10785 LitcelmorcelliAinda não há avaliações
- Oleo de Amendoa DoceDocumento1 páginaOleo de Amendoa DocecelmorcelliAinda não há avaliações
- Boletim Mascara FacialDocumento2 páginasBoletim Mascara FacialcelmorcelliAinda não há avaliações
- CamuCamu HG LitDocumento1 páginaCamuCamu HG LitcelmorcelliAinda não há avaliações
- Óleo Essencial de BergamotaDocumento1 páginaÓleo Essencial de BergamotacelmorcelliAinda não há avaliações
- Óleo Essencial de CitronelaDocumento2 páginasÓleo Essencial de CitronelacelmorcelliAinda não há avaliações
- Grupos Tec 2 20091OKDocumento2 páginasGrupos Tec 2 20091OKcelmorcelliAinda não há avaliações
- Vegecomplex® VC-FVDocumento2 páginasVegecomplex® VC-FVcelmorcelliAinda não há avaliações
- Alcool CetoestearilicoDocumento1 páginaAlcool CetoestearilicocelmorcelliAinda não há avaliações
- GUARANADocumento1 páginaGUARANAcelmorcelliAinda não há avaliações
- Cacau HG 10801 LitDocumento1 páginaCacau HG 10801 LitcelmorcelliAinda não há avaliações
- CastanhadaIndia OLDocumento1 páginaCastanhadaIndia OLcelmorcelliAinda não há avaliações
- FlavonidesDocumento2 páginasFlavonidescelmorcelliAinda não há avaliações
- MELANCIADocumento1 páginaMELANCIAcelmorcelliAinda não há avaliações
- Amora HGDocumento1 páginaAmora HGcelmorcelliAinda não há avaliações
- MentaPiperita HG 10910 LitDocumento1 páginaMentaPiperita HG 10910 LitcelmorcelliAinda não há avaliações
- Boletim Lauril Sulfato de Sódio PóDocumento1 páginaBoletim Lauril Sulfato de Sódio PócelmorcelliAinda não há avaliações
- Bacter Quick FTDocumento1 páginaBacter Quick FTJoão Paulo CastanheiraAinda não há avaliações
- Fispq Klyo Oxy Rev.01-16Documento9 páginasFispq Klyo Oxy Rev.01-16MarcoAinda não há avaliações
- Fisiologia Dos Animais Domésticos I - Apresentação HomeostaseDocumento16 páginasFisiologia Dos Animais Domésticos I - Apresentação Homeostasebruno do carmoAinda não há avaliações
- Catalogo Schioppa Linha MXDocumento17 páginasCatalogo Schioppa Linha MXJose luiz coelhoAinda não há avaliações
- Exercícios de Revisão BiocelDocumento115 páginasExercícios de Revisão BiocelMaria Rosa DmengeonAinda não há avaliações
- 90430Documento20 páginas90430Guilherme SouzaAinda não há avaliações
- Análise de Patologias Decorrentes de Infiltrações Nas EdificaçõesDocumento47 páginasAnálise de Patologias Decorrentes de Infiltrações Nas EdificaçõesTeofilo NhapuloAinda não há avaliações
- Certificado CompostoDocumento35 páginasCertificado CompostoVinicius SantanaAinda não há avaliações
- 2009 - MONTEIRO SILVA - Aplicações Industriais Da Biotecnologia EnzimáticaDocumento15 páginas2009 - MONTEIRO SILVA - Aplicações Industriais Da Biotecnologia EnzimáticaJuliana BrandAinda não há avaliações
- AtividadeLab1 - Osmose Discussão - CCDocumento3 páginasAtividadeLab1 - Osmose Discussão - CCjosecancelaAinda não há avaliações
- Estudo Dirigido Phmetria BiomedicinaDocumento2 páginasEstudo Dirigido Phmetria BiomedicinaManuella PimentaAinda não há avaliações
- FISPQ - Exxon - Isopar L FISPQDocumento11 páginasFISPQ - Exxon - Isopar L FISPQAlexAntonioPradoAinda não há avaliações
- Fispq - Nubira Synth 100-hDocumento4 páginasFispq - Nubira Synth 100-hDalia Weschenfelder SteffenAinda não há avaliações
- 2°série - QUI - ALUNO - 1°BI - WENDELL LEONARDO CARDOSODocumento34 páginas2°série - QUI - ALUNO - 1°BI - WENDELL LEONARDO CARDOSOwendell cardosoAinda não há avaliações
- 14º Simulado Enem (Ari de Sá) - 2º DiaDocumento38 páginas14º Simulado Enem (Ari de Sá) - 2º Diamaria matosAinda não há avaliações
- Exercícios - Aminoácidos e Proteínas 2018Documento6 páginasExercícios - Aminoácidos e Proteínas 2018walas joãoAinda não há avaliações
- Questões Sobre Administração de Medicamentos e Vias de Administraçã RespostasDocumento4 páginasQuestões Sobre Administração de Medicamentos e Vias de Administraçã RespostasKaline MunizAinda não há avaliações
- Bioquímica Aplicada À Saúde-Unidade 2-2.3-1ºsem2022-FolhetosDocumento5 páginasBioquímica Aplicada À Saúde-Unidade 2-2.3-1ºsem2022-FolhetosKauanna MartinsAinda não há avaliações
- Endurecimento AulaDocumento86 páginasEndurecimento AulaIgor HudsonAinda não há avaliações
- Relatório 02 de Energias de BiomassaDocumento11 páginasRelatório 02 de Energias de BiomassaVital Batista VitalAinda não há avaliações
- Manual Unidade CondensadoraDocumento16 páginasManual Unidade CondensadoraRicardo LimaAinda não há avaliações
- Concentração Micelar CríticaDocumento8 páginasConcentração Micelar CríticaLuísa De Melo ArrudaAinda não há avaliações
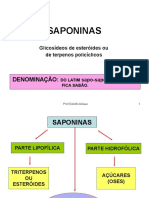
- Saponinas - FarmácognosiaDocumento60 páginasSaponinas - FarmácognosiaDiomara AlvesAinda não há avaliações